产品单价 |
面议 |
起订量 |
1 |
供货总量 |
不限量 |
发货期限 |
自买家付款之日起3天内发货 |
品牌 |
轮椅UKCA |
病床UKCA |
助行器UKCA |
英国脱欧已经2年,原来欧盟的MDR CE已经不适用于出口英国,因此办理英国UKCA势在必行,完成英国MHRA注册,英代UKRP是之路。
康复器材电动轮椅,手动轮椅,助行器,病床等产品在英国拥有广大的市场,完成合规的UKCA 才能避免清关风险。
出口英国的医疗器械的合格评定依据是 UK MDR 2002, 该法规基本沿用欧盟旧指令93/42 MDD,因此康复辅助器械,例如手动轮椅、电动轮椅和代步车,均被归类为 I 类医疗器械。
目前I 类医疗器械打上CE或者UKCA标志后即可进入英国市场。2023年6月30日后,I 类医疗器械打上UKCA标志方可出口英国。那么制造商想要给医疗器械加贴UKCA标志,需要做些什么呢?
的UK Responsible Person(UKRP)
要将医疗产品投放到英国市场(英格兰、威尔士和苏格兰),英国境外的制造商的UKRP。
值得注意的是,在欧盟市场,不同的产品可以不同的欧盟授权代表,但是在英国,制造商只能的UKRP。
UKRP在MHRA完成了产品注册
UKRP需要向MHRA递交产品注册申请。对于I 类康复辅助器械,注册申请材料包括:
1. UKRP的协议;
2. 说明书;
3. 符合性声明;
4. 标签;
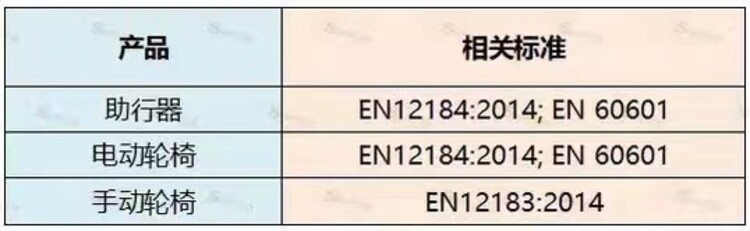
5. 相关专标报告
(以本文的产品为例,需要提交以上标准的报告,SUNGO实验室可开展轮椅和代步车的性能检测并提供相关报告,为客户顺利拿到英国出口资质提供有效文件)。
以下是我们客户的电动轮椅出口英国的时候遇到的调查案例。电动轮椅上坡时发生倾翻,英国当局要求提供测试数据和测试报告。
》》产品有全套测试报告,证明是客户误用导致的事故,制造商免责。因此,开展产品检测,获得的测试报告尤其重要。
以下是注册成功的电动轮椅MHAR英国药监局批准信函:

有符合要求的CE技术文件或
UKCA技术文件
鉴于2023年6月30日,I 类医疗器械强制要求满足UKCA的要求,建议广大制造商尽早准备。
完成的UKCA技术文件需要交给UKRP保存,以备英国调查需要及时提供。
| 上海沙格企业管理咨询有限公司广州分公司 | |||
|---|---|---|---|
| 联系人 | 王瑞芬 |
微信 | 无 |
| 手机 | ����������� | 邮箱 | 81042498@qq.com |
| 传真 | 无 | 地址 | 广州市天河区天河北路620号2604房,2603房(仅限办公用途) |
| 主营产品 | 美国fda注册,欧盟ce认证 | 网址 | /qiye2884368/ |





