产品单价 |
1.00元 |
起订量 |
1000 |
供货总量 |
10000 |
发货期限 |
自买家付款之日起3天内发货 |
品牌 |
试剂CE |
核酸检测试剂CE |
抗原试剂CE |
IVDR延期了,给与IVDD 试剂厂家出口欧盟的缓冲器。近日很多试剂厂家纷纷办理欧盟CE,以获得欧盟市场的份额。
核酸检测试剂CE,抗原检测试剂CE,中和抗体检测试剂CE,病毒采样管CE,采样拭子CE流程是怎么样的呢?
IVDD CE延期内容
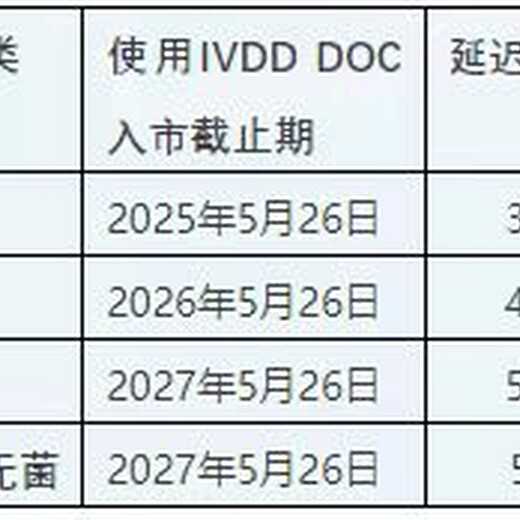
1. 根据IVDD指令98/79/EC获得公告机构CE证书的IVD器械(List A, List B, 自测类器械)晚使用期限为2025年5月26日。
2. 根据IVDD指令98/79/EC无需公告机构介入,而在新的IVDR法规2017/746需要公告机构开展合格评定的器械:


特别关注:
1)虽然IVDR的实施日期延迟,但使用IVDD DOC投放市场使用的IVD产品,其上市后监督,在2022年5月26日开始就应参照IVDR法规中上市后监督相应的要求实施。
2)在IVDD属于OTHER类别同时在新版IVDR法规里属于自我声明的A类非灭菌器械依然需在2022年5月26日前完成转换。

PART 3 应对措施
对于IVDD和IVDR均不需要公告机构参与的IVD器械制造商,应尽快按照IVDR 2017/746来完成合规程序。程序包括:
1) 按照IVDR 2017/746编制技术文件;
2) 欧盟授权代表;
3) 完成IVDR 2017/746器械注册;
4) 发布DOC文件;
5) 按照IVDR 2017/746执行上市后监督体系。
对于IVDD不需要公告机构参与,但是IVDR需要公告机构参与的IVD器械制造商,应尽快(在2022年5月26日之前)按照IVDD来完成DOC以获得缓冲期资格。
程序包括:
1) 按照IVDD 98/79/EC编制技术文件;
2) 欧盟授权代表;
3) 完成IVDD 98/79/EC器械注册;
4) 发布DOC文件;
5) 按照IVDR 2017/746执行上市后监督体系。
IVDD CE办理周期3~4周(含欧盟注册,欧代,CE技术文件)
| 上海沙格企业管理咨询有限公司广州分公司 | |||
|---|---|---|---|
| 联系人 | 王瑞芬 |
微信 | 无 |
| 手机 | ����������� | 邮箱 | 81042498@qq.com |
| 传真 | 无 | 地址 | 广州市天河区天河北路620号2604房,2603房(仅限办公用途) |
| 主营产品 | 美国fda注册,欧盟ce认证 | 网址 | /qiye2884368/ |